Energía de activación Calcular K de la ecuación de Arrhenius a una temperatura determinada
La ecuación de Arrhenius es k = Ae^ (-Ea/RT), donde A es la frecuencia o el factor pre-exponencial y e^ (-Ea/RT) representa la fracción de las colisiones que tienen suficiente energía para superar la barrera de activación (es decir, tienen mayor o igual energía que la energía de activación Ea) a temperatura T. Esta ecuación se puede usar para co.
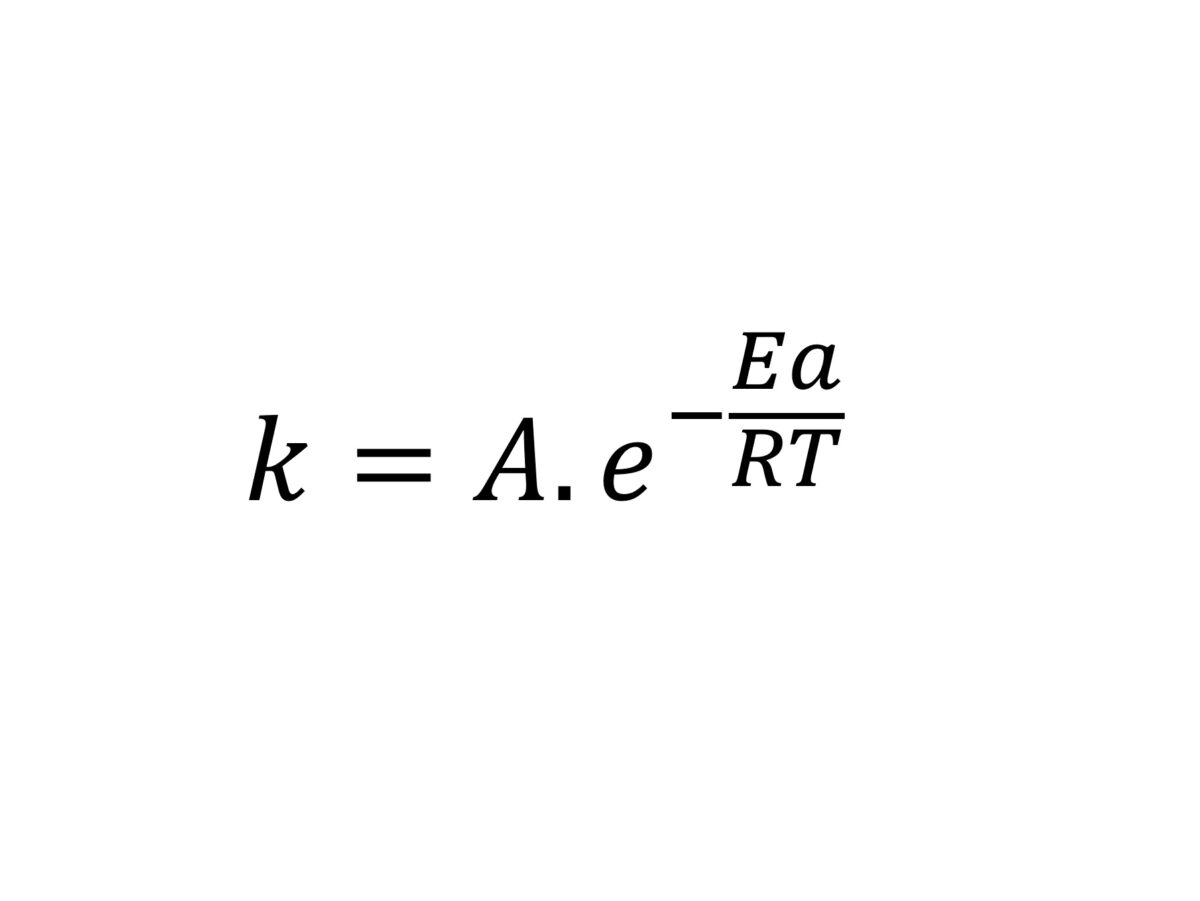
Ecuación de Arrhenius Teoría, ejemplos y más
La ecuación de Arrhenius tiene las siguientes dos expresiones: K = Ae-Ea/RT Forma de la ecuación usada en química y que está relacionada con los moles de reactivo. K = Ae-Ea/kBT Forma de la ecuación usada en física y que está relacionada con las moléculas más, que con los moles.

Arrhenius ecuación YouTube
Arrhenius también se destacó como prolífico escritor, con la publicación de obras y discursos académicos. - Electroquímica Teórica (1900). - Tratado de Física Cósmica (1903). - Teoría de la Química, la Tierra y el Universo (1906). - Inmunoquímica (1907).

Formas de la ecuación de Arrhenius YouTube
La ecuación de Arrhenius es una expresión matemática que se utiliza para comprobar la dependencia de la constante de velocidad (o cinética) de una reacción química con respecto a la temperatura a la que se lleva a cabo esa reacción. 1 La ecuación fue propuesta primeramente por el químico neerlandés J. H. van 't Hoff en 1884; cinco años después.

Ecuación de Arrhenius El efecto de la temperatura Sánchez Flores M. Instituto Tecnológico de
La ecuación de Arrhenius muestra que k cambia con. Ea y T Para ver cómo k cambia con la temperatura usa el forma integrada de la ecuación de Arrhenius. Ln (k2/k1) = (Ea/R) (1/T1 - 1/T2) Este video contiene la solución al siguiente problema: Si k = 2.15 x 10-8 1/m∙s a 650 K y la energía de activación es 182 kJ/mol ¿cuál sería k a 700 K?
/GettyImages-92831471-5c56435846e0fb00012ba77a.jpg)
Ácidos y Bases de Arrhenius Historia F+Q
Finalmente, en 1899, el químico sueco Svante Arrhenius (1859-1927) combinó los conceptos de energía de activación y la ley de disribución de Boltzmann en una de las relaciones más importantes en la química física: Tómate un momento para enfocarte en el significado de esta ecuación, descuidando por el momento el factor A.

Representación gráfica de la ecuación de Arrhenius para la... Download Scientific Diagram
veamos cómo utilizar la ecuación de arrhenius para encontrar la energía de activación de una reacción en este ejemplo nuestra reacción es la hizo meditación de metil isocianato que lo tenemos del lado izquierdo y se transforma en el y somero acetonitrilo esta es una reacción de primer orden y aquí tenemos las diferentes constantes de velocidad a.

Linealización de la ecuación de Arrhenius para combustión de metano... Download Scientific Diagram
La ecuación de Arrhenius es una expresión matemática que se utiliza para comprobar la dependencia de la constante de velocidad (o cinética) de una reacción química con respecto a la temperatura a la que se lleva a cabo esa reacción.[1]
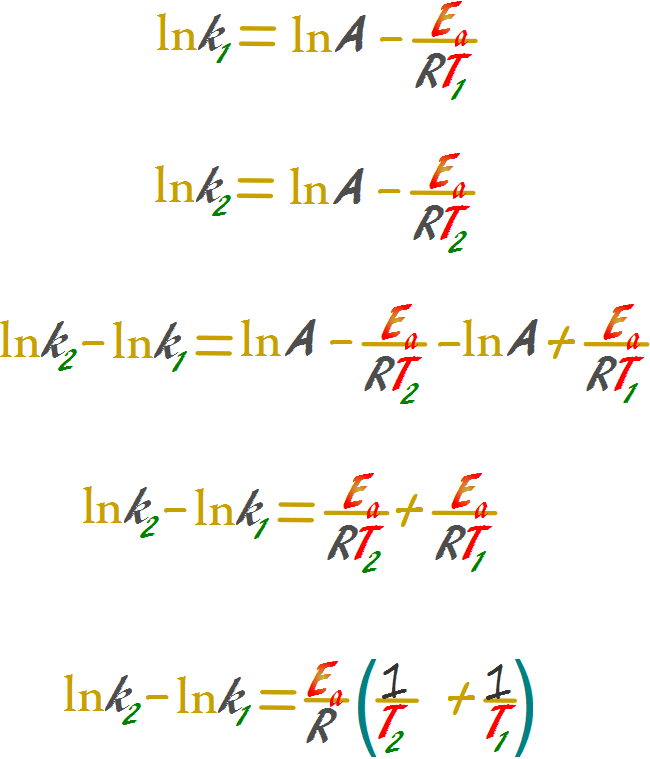
Ecuación de Arrhenius Paperblog
La ecuación de Arrhenius tiene las siguientes dos expresiones: La forma de las ecuaciones utilizadas en química, relacionadas con el número de moles de los reactivos. Formas de ecuaciones utilizadas en física, que se relacionan con moléculas en lugar de moles.

EJERCICIO ECUACIÓN DE ARRHENIUS PARA DOS TEMPERATURAS DISTINTAS Mediateca de EducaMadrid
Solución: Utilizando la ecuación de Arrhenius, podemos despejar el factor de preexponencial A: k = A * e(-Ea/RT) A = k / e (-Ea/RT) Sustituyendo los valores conocidos: A = (2.5 * 10 -4 s -1) / e (-50 * 103 J/mol / (8.314 J/ (mol*K) * 300 K) Calculando el valor numérico: A ≈ 1.16 * 10 9 s -1
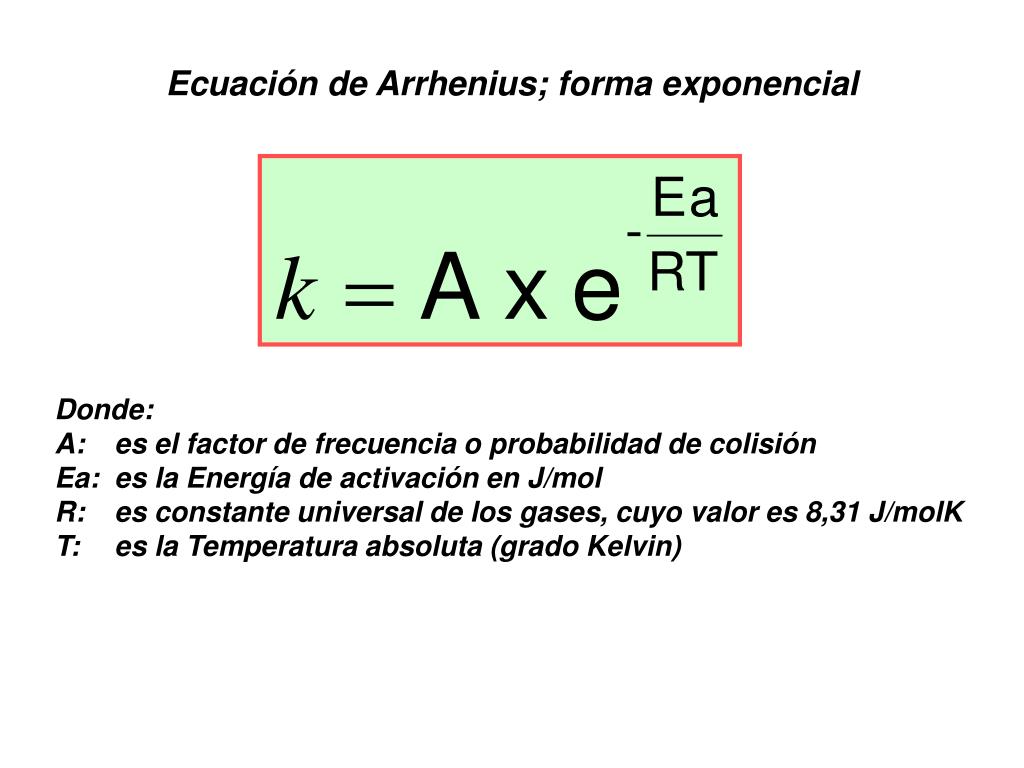
PPT Cinética Química PowerPoint Presentation, free download ID5823969
La ecuación de Arrhenius es una expresión matemática que se utiliza para comprobar la dependencia de la constante de velocidad (o cinética) de una reacción química con respecto a la temperatura a la que se lleva a cabo esa reacción.

Ecuación de Arrhenius YouTube
The exponential term in the Arrhenius equation implies that the rate constant of a reaction increases exponentially when the activation energy decreases. Because the rate of a reaction is directly proportional to the rate constant of a reaction, the rate increases exponentially as well. Because a reaction with a small activation energy does not.

Ecuacion de Arrhenius Aplicacion de la EAplicación de la Ecuación de Arrhenius utilizada para la
De forma sencilla, la ecuación de Arrhenius muestra la dependencia de la constante de velocidad k, de las reacciones químicas a una temperatura T y la energía de activación Ea de acuerdo con la expresión: Donde, k: es la constante cinética (depende de la temperatura) A: es el factor preexponencial o factor de frecuencia.

Concentración, Tiempo de vida media, Presión, Orden de Reacción, Velocidad de reacción, Temperatura
ya vimos una de las formas de la ecuación de arrhenius que dice que la constante de velocidad que es igual al factor de frecuencia a por el elevada a menos sobre rt donde el a es la energía de activación r es la constante de los gases y t es la temperatura pero existen otras formas de esta ecuación que podemos usar dependiendo del problema vamos.

Conclusión Factor preexponencial de la ecuación de Arrhenius La energía de activación suele
La ecuación de Arrhenius es una representación matemática utilizada para expresar la dependencia de la constante cinética de una reacción química con la temperatura a la cual puede llevarse a cabo esta reacción.

Energía De Activación, La Química, Ecuación De Arrhenius imagen png imagen transparente
Tomando el logaritmo natural de la ecuación de Arrhenius y reorganizando los términos se obtiene una ecuación que tiene la misma forma que la ecuación de una línea recta (y = mx+b): ln (k) = -E a /R (1/T) + ln (A) En este caso, la "x" de la ecuación lineal es el recíproco de la temperatura absoluta (1/T). Entonces, cuando se toman datos.